Drei Wissenschaftler wurden für die Entdeckung einer neuen Form molekularer Architektur mit dem Nobelpreis für Chemie 2025 ausgezeichnet: Kristalle, die große Hohlräume enthalten.
Susumu Kitagawa von der Kyoto University, Japan, Richard Robson von der University of Melbourne, Australien, und Omar M. Yaghi von der University of California, Berkeley, in den USA, teilen sich eine Preissumme von 11 Millionen schwedischen Kronen (£870.000).
Der Preis würdigt die bahnbrechenden Beiträge der drei Wissenschaftler bei der Entwicklung sogenannter metallorganischer Gerüste (Metal-Organic Frameworks, Mofs). Mofs sind eine vielfältige Klasse kristalliner Materialien, die aufgrund des Vorhandenseins mikroskopisch kleiner offener Hohlräume in ihren Strukturen in der Chemie große Aufmerksamkeit erregt haben. Sie tragen dazu bei, umweltfreundliche Technologien zu revolutionieren, beispielsweise die Gewinnung von Wasser aus der Wüstenluft und die Abscheidung von CO₂.
Die Breite der Hohlräume kann von einigen Angström (ein Angström ist eine Längeneinheit, die einem Hundertmillionstel Zentimeter entspricht) bis zu mehreren Nanometern (ein Millionstel Millimeter) reichen. Das bedeutet, dass sie viel zu klein sind, um sie mit bloßem Auge oder sogar mit den meisten Mikroskopen zu erkennen. Aber sie haben die perfekte Größe, um verschiedene Moleküle unterzubringen.
Die Entwicklung von Mofs lässt sich bis in die späten 1950er Jahre zurückverfolgen, als Forscher begannen, „Koordinationspolymere“ zu entdecken. Hierbei handelt es sich um Materialien, die aus verknüpften Ketten von Metallionen (Atomen, die Elektronen verloren oder aufgenommen haben) und kohlenstoffbasierten Brückenmolekülen, sogenannten Linkern, bestehen. Diese Materialien enthielten keine Hohlräume, basierten jedoch auf der gleichen metallorganischen Chemie, aus der später Mofs hervorgingen.
In den späten 1980er Jahren berichtete Robsons Forschungsgruppe, dass einige Koordinationspolymere als gerüstartige Strukturen hergestellt werden könnten, bei denen die kohlenstoffbasierten Linker vor allem dreidimensionale Anordnungen um Cluster flüssiger Lösungsmittelmoleküle bildeten. Wie in Robsons Forschungsartikel erwähnt, offenbarte dies „eine ungewöhnliche Situation, in der etwa zwei Drittel des Inhalts dessen, was zweifellos ein Kristall ist, tatsächlich flüssig sind“.
Mitte/Ende der 1990er Jahre demonstrierte Yaghis Gruppe, dass es möglich ist, Koordinationspolymere herzustellen, die ihre Strukturen auch dann beibehalten, wenn die Lösungsmittelmoleküle aus den Hohlräumen entfernt wurden. Dies war ein überraschendes Ergebnis, das die vorherrschende Annahme widerlegte, dass solche Gerüste fragil seien und zusammenbrechen würden, wenn das Lösungsmittel entfernt würde.
1997 zeigte Kitigawas Forschungsgruppe, dass die offenen Hohlräume zur Aufnahme von Gasmolekülen genutzt werden könnten. Er zeigte auch, dass sich in vielen Fällen das Gerüst selbst ausdehnt, wenn Gasmoleküle darin absorbiert werden, und sich zusammenzieht, wenn sie freigesetzt werden. Diese Koordinationspolymere mit permanenten, offenen Hohlräumen wurden als Mofs bekannt.
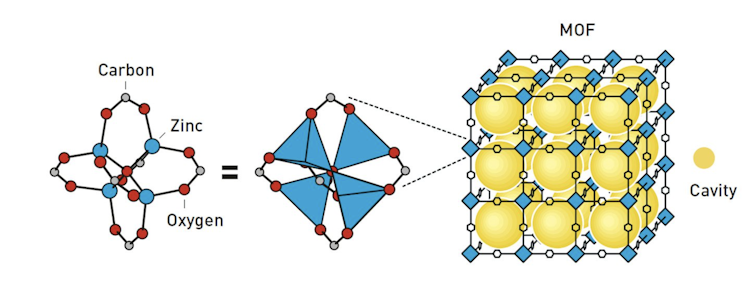
Die Entdeckungen der drei Wissenschaftler markierten praktisch die Geburtsstunde der modernen MOF-Chemie, und seitdem wurden viele tausend Forschungsartikel zu ihnen veröffentlicht.
Breites Anwendungsspektrum
Warum sind Mofs für Chemiker so interessant? Die mikroskopisch kleinen Hohlräume in MOFs bieten einen einzigartigen und kontrollierbaren Ort, an dem die Chemie stattfinden kann. Eine Schlüsselanwendung von Mofs ist die Gasspeicherung. In vielen Fällen können diese Materialien Gase in viel höherer Dichte halten als in ihrem freien gasförmigen Zustand.
Dies bietet erhebliche Vorteile für grüne Technologien wie Fahrzeuge mit Brennstoffzellenantrieb, bei denen der Wasserstoff-Kraftstoff möglichst effizient transportiert werden muss. Viele Mofs eignen sich besonders gut für bestimmte Gase, was bedeutet, dass sie auch dabei helfen können, Gasgemische in Abgasströmen zu trennen oder CO₂ aus der Luft abzuscheiden, um die Auswirkungen der globalen Erwärmung abzumildern.
Mofs können auch als wirksame Katalysatoren für chemische Reaktionen in den Hohlräumen wirken. Einer der Hauptvorteile von Mofs als Katalysatoren besteht darin, dass es für Chemiker relativ einfach ist, die Metalle und kohlenstoffbasierten Linker zu wechseln und auszutauschen, um die Eigenschaften auf einen bestimmten Zweck abzustimmen.
Neben Gasmolekülen können Mofs auch andere kleine Moleküle wie Arzneimittel aufnehmen. Dies bedeutet, dass sie zur Lagerung und Abgabe von Arzneimitteln an ein bestimmtes Ziel verwendet werden können, wobei ihre poröse Beschaffenheit eine kontrollierte Freisetzung therapeutischer Chemikalien ermöglicht.
In den letzten Jahren haben sich MOFs für viele andere Anwendungen als vielversprechend erwiesen, darunter Batterien, thermische Energiespeicher und chemische Sensoren (Geräte, die Chemikalien wie Verunreinigungen überwachen und erkennen können). Spannenderweise gibt es noch viele andere Anwendungen, die noch erforscht werden müssen.
Obwohl Mofs bereits vor über drei Jahrzehnten entdeckt wurden, sind sie nach wie vor eines der heißesten Forschungsgebiete in der Materialchemie und werden dies zweifellos auch in den kommenden Jahren tun.
John Griffin, Professor für Materialchemie, Lancaster-Universität
wird von The Conversation unter einer Creative Commons-Lizenz erneut veröffentlicht.

